刘颖课题组揭示HLH-11/TFAP4响应营养物质水平调控脂质代谢
2020年11月24日,北京大学分子医学研究所刘颖课题组在Nature Communications发表了题为“?HLH-11 modulates lipid metabolism in response to nutrient availability”的研究论文,揭示秀丽隐杆线虫转录调控蛋白HLH-11及其哺乳动物同源蛋白TFAP4能够感知营养条件,调控脂质代谢。
感知环境中可供利用的营养物质水平,并根据营养条件变化对自身代谢作出适应性地调控,对于机体的生存至关重要。脂质是机体储存能量的重要形式。在食物缺乏的情况下,快速有效的利用脂质供能可以为机体提供生存优势,因此该机制在物种间具有保守性。环境中营养物质水平的变化能够调控脂质代谢相关酶的转录,导致代谢的重编程。有研究表明,转录因子HLH-30/TFEB,核激素受体NHR-49/PPARα等能够在食物缺乏的情况下,通过调节脂质代谢相关基因的转录,促进脂质的分解供能。然而,对于营养条件对脂质代谢调控的理解还需要更近一步的研究。
本研究利用秀丽线虫为模型,通过构建可以响应饥饿的荧光报告体系进行遗传筛选,发现转录调控蛋白HLH-11在饥饿引起脂质分解的过程中起了关键的调控作用:HLH-11对脂质分解相关基因的表达具有转录抑制作用。饥饿能够引起HLH-11蛋白水平下调,从而激活脂质分解代谢基因的转录,促进脂质分解(图1)。同时,在哺乳动物细胞中,HLH-11的同源蛋白TFAP4也能够感知营养条件并且调节脂质代谢,说明营养条件对脂质代谢的调控机制在物种间具有保守性。这项研究成果对于脂质代谢疾病的治疗具有潜在应用。
北京大学前沿交叉学科研究院、生命科学联合中心博士研究生李怡为论文第一作者,分子医学研究所刘颖研究员为论文的通讯作者。分子医学研究所博士后丁晚秋、研究员李川昀参与了论文的部分工作。
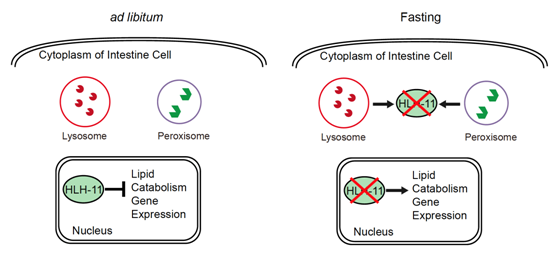
| 图1. (左)正常喂食情况下,HLH-11抑制脂质分解相关基因的转录; (右)饥饿状态下,HLH-11被溶酶体和蛋白酶体途径降解,解除了脂质分解相关基因的转录抑制,促进脂质分解供能。
|
附件下载:
