2021年7月21日,刘颖研究组在Nature杂志在线发表题为“SAR1B senses leucine levels to regulate mTORC1 signalling”的研究论文。报道了一个全新的亮氨酸受体蛋白SAR1B,及其通过mTORC1调控非小细胞肺癌发生的机制。
研究人员结合免疫共沉淀和质谱技术鉴定到亮氨酸受体蛋白SAR1B。SAR1B的经典功能是作为G蛋白酶参与囊泡形成,并与其他四个亚基共同组装成COPII复合物,在内质网向高尔基体递送物质的过程中发挥重要作用[1]。研究人员发现,SAR1B感知亮氨酸的过程并不依赖于其经典的小G蛋白酶活性。
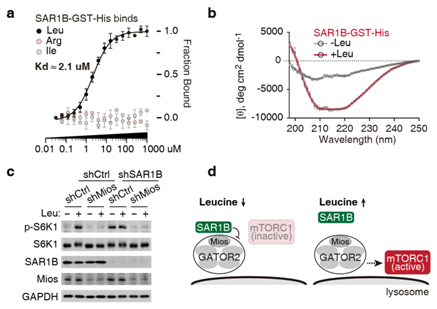
体外实验表明,SAR1B能够直接结合亮氨酸(图1a),并在结合亮氨酸后发生构象转变(图1b)。细胞实验表明,SAR1B感受到亮氨酸信号后,通过GATOR2复合物将信号传递给mTORC1;敲低GATOR2复合物的组分Mios,将阻断亮氨酸信号的传递(图1c)。综合诸多实验结果,研究人员总结如下:在亮氨酸缺乏时,SAR1B结合并抑制GATOR2复合物(GATOR2是维持mTORC1活化的重要因子),mTORC1失活。当氨基酸充足时,SAR1B结合亮氨酸,发生变构,随后与GATOR2解离,被解放的GATOR2进而激活mTORC1(图1d)。此外,研究人员还利用无脊椎模式生物线虫,证明了SAR1B感知亮氨酸是进化上高度保守的。
图1. 亮氨酸感知机制。 (a) SAR1B体外结合亮氨酸。(b) SAR1B结合亮氨酸变构。(c) SAR1B通过与GATOR2复合物中的Mios蛋白互作调控mTORC1活性。(d)亮氨酸缺乏时,SAR1B抑制GATOR2,mTORC1失活。亮氨酸充足时,SAR1B解离GATOR2,mTORC1被激活。
值得一提的是,此前已有一个亮氨酸受体蛋白Sestrin2被报道[2]。研究人员从以下四个方面阐明了这两个受体蛋白的不同之处。(1)它们结合在GATOR2的不同亚基上。SAR1B结合Mios亚基,而Sestrin2结合Seh1L亚基。(2)它们对亮氨酸的敏感程度不同,SAR1B能够感知到更低浓度的亮氨酸,亲和力为Kd ≈ 2 μM。而Sestrin2感知相对高浓度的亮氨酸,亲和力为Kd ≈ 20 μM。(3)它们识别不同的亮氨酸结构特征。SAR1B识别的是亮氨酸的氨基端和侧链,能够容忍羧基端修饰。而Sestrin2则识别亮氨酸的氨基端和羧基端,能够部分容忍侧链修饰。(4)两个受体蛋白存在组织分布差异性,且在肌肉中,两个受体协同调控mTORC1。关于这点,研究人员进行了深入探索。
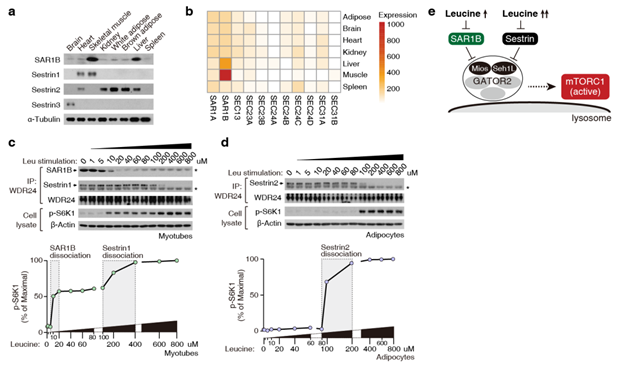
SAR1B在骨骼肌中丰度最高(图2a),且其表达不依赖于CopII复合物的其他四个亚基(图2b),暗示其存在不依赖于囊泡运输的新功能。骨骼肌中,Sestrin家族另一成员Sestrin1(功能等同Sestrin2)也表达(图2a)。在脂肪组织中,仅Sestrin2高表达(图2a)。功能与受体分布情况一致,肌肉细胞中,SAR1B和Sesrtrin1先后从GATOR2解离,促成了mTORC1 “二次”激活效应(图2c)。而脂肪细胞中,仅Sestrin2对mTORC1进行了“一次”调控(图2d)。综上,亮氨酸受体SAR1B和Sestrin协作共同调控mTORC1信号(图2e)。
图2. 亮氨酸受体SAR1B和Sestrin协同调控mTORC1。 (a) SAR1B和Sestrin1在骨骼肌高表达;Sestrin2在脂肪高表达。(b) SAR1B区别于CopII其他亚基单独在骨骼肌高表达。(c, d) 肌肉和脂肪细胞中亮氨酸感知的差异。(e) SAR1B和Sestrin协同调控mTORC1。
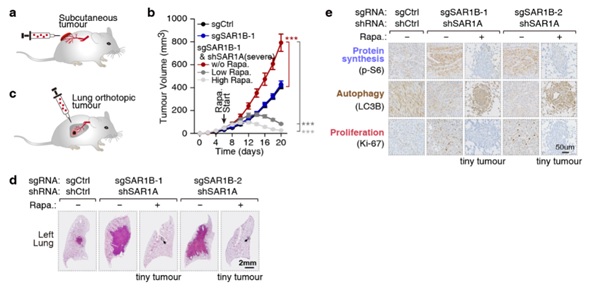
最后,研究人员通过生物信息学分析,发现SAR1B-mTORC1信号在人类非小细胞肺癌中扮演潜在作用,并随后建立了裸鼠肿瘤模型证明了该假设。失去SAR1B及其同源蛋白SAR1A将促进小鼠皮下瘤(图3a, b)和肺内原位瘤(图3c, d)发生,给小鼠注射mTORC1抑制剂雷帕霉素(Rapa.)可阻止肿瘤发生(图3b, d)。此外,肺切片和免疫组化染色结果表明,失去SAR1A/B将促进肿瘤代谢重编程(合成代谢加速,分解代谢抑制),增强肿瘤细胞增值能力(图3e)。因此,SAR1B在肺癌中发挥着潜在抑癌因子的作用。
图3. 肿瘤病理意义。(a) 皮下瘤模型。(b) 失去SAR1A/B促进mTORC1依赖的皮下瘤生长。(c)原位瘤模型。(d, e) 失去SAR1A/B促进mTORC1依赖的原位瘤生长(d)和肿瘤代谢重编程(e)。
综上,研究人员发现了一个全新的亮氨酸受体蛋白SAR1B,并详细解析了其感应亮氨酸调控mTORC1信号的分子机制。通过生物信息学分析和建立裸鼠原位瘤模型,研究人员证明了SAR1B是一个潜在的人类非小细胞肺癌抑癌因子,有希望成为非小细胞肺癌的新型生物标志物,为非小细胞肺癌的治疗提供新的药物靶标。
参考文献
[1] Zanetti, G., Pahuja, K. B., Studer, S., Shim, S. & Schekman, R. COPII and the regulation of protein sorting in mammals. Nat Cell Biol 14, 20-28, doi:10.1038/ncb2390 (2011).
[2] Wolfson, R. L. et al. Sestrin2 is a leucine sensor for the mTORC1 pathway. Science 351, 43-48, doi:10.1126/science.aab2674 (2016).
原文链接:https://www.nature.com/articles/s41586-021-03768-w